Resumo
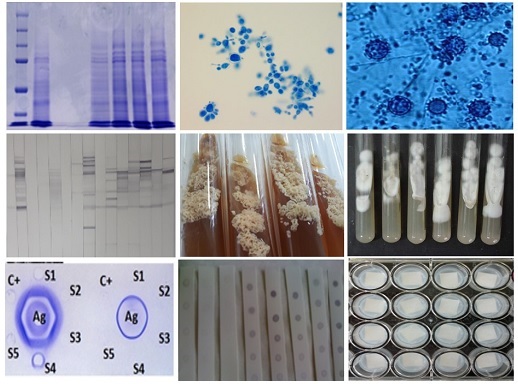
The standardization and validation of a multiplex assay requires the combination of important parameters such as sensitivity and specificity, acceptable levels of performance, robustness, and reproducibility. We standardized a multiparametric Dot-blot aimed at the serological screening of paracoccidioidomycosis, histoplasmosis, and aspergillosis. A total of 148 serum were evaluated: 10 from healthy subjects, 36 from patients with paracoccidioidomycosis, 62 from patients with histoplasmosis, and 40 from patients with aspergillosis. It was found that the multiparametric Dot-blot showed a high percentage of cross-reactivity. However, when evaluated individually, in the serological screening of histoplasmosis, a good performance was observed when compared to the double immunodiffusion assay, considered the gold standard test, with 100% co-positivity and 83.3% co-negativity. The performance of serological screening for aspergillosis was not satisfactory when compared to double immunodiffusion, showing 71.4% co-positivity and 100% co-negativity. The evaluation of the stability of nitrocellulose membranes showed that membranes sensitized with H. capsulatum antigen remained stable for 90 days and those sensitized with A. fumigatus antigen for 30 days. We conclude that the use of crude antigens was not suitable for the standardization of the multiparametric Dot-blot assay, due to the high cross-reactivity, and that further tests should be performed with purified proteins.
Referências
1. Bongomin F, Gago S, Oladele RO, Denning DW. Global and multi-national prevalence of fungal diseases – estimate precision. J Fungi. 2017;3(4):57. https://doi.org/10.3390/jof3040057
2. Silva-Ferreira C, de Castro Ribeiro EM, Miranda Goes AD, Mello Silva BD. Current strategies for diagnosis of paracoccidioidomycosis and prospects of methods based on gold nanoparticles. Future Microbiol. 2016;11:973-85. https://doi.org/10.2217/fmb-2016-0062
3. Almeida-Silva F, Gonçalves D, Abreu Almeida M, Guimarães AJ. Current aspects of diagnosis and therapeutics of histoplasmosis and future trends: moving onto a new immune (diagnosis and therapeutic) era? Curr Clin Micro Rpt. 2019;6:98-107. https://doi.org/10.1007/s40588-019-00118-3
4. Alvarado P, Pérez-Rojas Y, Zambrano EA, Gonzatti MI, Roschman-González A. Improved serodiagnosis of histoplasmosis by use of deglycosylated extracellular released antigens of Histoplasma capsulatum. J Microbiol Methods. 2020;175:105981. https://doi.org/10.1016/j.mimet.2020.105981
5. Latgé JP, Chamilos G. Aspergillus fumigatus and aspergillosis in 2019. Clin Microbiol Rev. 2019;33(1):e00140-18. https://doi.org/10.1128/CMR.00140-18
6. Volpe Chaves CE, do Valle Leone de Oliveira SM, Venturini J, Grande AJ, Silvestre TF, Poncio Mendes R et al. Accuracy of serological tests for diagnosis of chronic pulmonary aspergillosis: a systematic review and meta-analysis. PLoS One. 2020;15(3):e0222738. https://doi.org/10.1371/journal.pone.0222738
7. da Silva JF, de Oliveira HC, Marcos CM, Assato PA, Fusco-Almeida AM, Mendes-Giannini MJS. Advances and challenges in paracoccidioidomycosis serology caused by Paracoccidioides species complex: an update. Diagn Microbiol Infect Dis. 2016;84(1):87-94. https://doi.org/10.1016/j.diagmicrobio.2015.06.004
8. Pappas MG. Recent applications of the Dot-ELISA in immunoparasitology. Vet Parasitol. 1988;29(2-3):105-29. https://doi.org/10.1016/0304-4017(88)90120-3
9. Taborda CP Camargo ZP. Diagnosis of paracoccidioidomycosis by Dot immunobinding assay for antibody detection using the purified and specific antigen gp43. J Clin Microbiol. 1994;32(2):554-6. https://doi.org/10.1128/jcm.32.2.554-556.1994
10. Martins R, Marques S, Alves M, Fecchio D, de Franco MF. Serological follow-up of patients with paracoccidioidomycosis treated with itraconazole using Dot-blot, ELISA and Western-blot. Rev Inst Med Trop São Paulo. 1997;39(5):261-9. https://doi.org/10.1590/s0036-46651997000500004
11. Carvalho KC, Vallejo MC, Camargo ZP, Puccia R. Use of recombinant gp43 isoforms expressed in Pichia pastoris for diagnosis of paracoccidioidomycosis. Clin Vaccine Immunol. 2008;15(4):622-9. https://doi.org/10.1128/CVI.00437-07
12. Assunção TRS. Desenvolvimento de método para diagnóstico da paracoccidioidomicose humana utilizando antígeno recombinante de Paracoccidioides brasiliensis. [dissertação de mestrado]. Londrina (PR): Universidade Estadual de Londrina; 2012.
13. Kamikawa, CM, Mendes RP, Vicentini AP. Standardization and validation of Dot-ELISA assay for Paracoccidioides brasiliensis antibody detection. J Venom Anim Toxins Incl Trop Dis. 2017;23:11. https://doi.org/10.1186/s40409-017-0101-3
14. Shahid M, Malik A, Bhargava R. Prevalence of aspergillosis in chronic lung diseases. Indian J Med Microbiol. 2001;19(4):201-5.
15. Malik A, Shahid M, Bhargava R. Prevalence of aspergillosis in bronchogenic carcinoma. Indian J Pathol Microbiol. 2003;46(3):507-10.
16. Shahid M, Malik A, Bhargava R. Bronchogenic carcinoma and secondary aspergillosis common yet unexplored: evaluation of the role of bronchoalveolar lavage-polymerase chain reaction and some nonvalidated serologic methods to establish early diagnosis. Cancer. 2008;113(3):547-58. https://doi.org/10.1002/cncr.23570
17. Silva DF. Análise da estabilidade de exoantígenos de Paracoccidioides brasiliensis [dissertação de mestrado]. São Paulo (SP): Coordenadoria de Controle de Doenças da Secretaria de Estado da Saúde; 2005.
18. Bradford MM. A rapid and sensitive method for the quantitation of microgram quantities of protein utilizing the principle of protein-dye binding. Anal Biochem. 1976;72(1-2):248-254. https://doi.org/10.1006/abio.1976.9999
19. Freitas RS. Caracterização fenotípica e padronização de antígenos de H. capsulatum var. capsulatum para o diagnóstico da histoplasmose. [dissertação de mestrado]. São Paulo (SP): Coordenadoria de Controle de Doenças da Secretaria de Estado da Saúde; 2005.
20. Freitas RS, Kamikawa CM, Vicentini AP. Fast protocol for the production of Histoplasma capsulatum antigens for antibody detection in the immunodiagnosis of histoplasmosis. Rev Iberoam Micol. 2018:35(1):27-31. https://doi.org/10.1016/j.riam.2017.04.004
21. Kamikawa CM. Padronização da metodologia de Dot-blot para o diagnóstico rápido da paracoccidioidomicose. [dissertação de mestrado]. São Paulo (SP): Coordenadoria de Controle de Doenças da Secretaria de Estado da Saúde; 2014.
22. Ouchterlony O. Antigen-antibody reactions in gels. Acta Path Microbiol Scand. 1949;26(4):507-15. https://doi.org/10.1111/j.1699-0463.1949.tb00751.x
23. Gorocica P, Taylor ML, Alvarado-Vásquez N, Pérez-Torres A, Lascurain R, Zenteno E. The interaction between Histoplasma capsulatum cell wall carbohydrates and host components: relevance in the immunomodulatory role of histoplasmosis. Mem Inst Oswaldo Cruz. 2009;104(3):492-6. https://doi.org/10.1590/s0074-02762009000300016
24. Gow NAR, Latge JP, Munro CA. The fungal cell wall: structure, biosynthesis, and function. Microbiol Spectr. 2017;5(3). https://doi.org/10.1128/microbiolspec.FUNK-0035-2016
25. Garcia-Rubio R, de Oliveira HC, Rivera J, Trevijano-Contador N. The fungal cell wall: candida, Cryptococcus, and Aspergillus species. Front Microbiol. 2020;10:2993. https://doi.org/10.3389/fmicb.2019.02993
26. Connolly PA, Durkin MM, Lemonte AM, Hackett EJ, Wheat LJ. Detection of histoplasma antigen by a quantitative enzyme immunoassay. Clin Vaccine Immunol. 2007;14(12):1587-91. https://doi.org/10.1128/CVI.00071-07
27. Sato H, Honigman AS, Scalarone GM. Development of a comparative Dot-ELISA for the detection of antibodies in blastomycosis. Diagn Microbiol Infect Dis. 1987;7(1):37-43. https://doi.org/10.1016/0732-8893(87)90067-8
28. Mendes-Giannini MJ, Camargo ME, Lacaz CS, Ferreira AW. Immunoenzymatic absorption test for serodiagnosis of paracoccidioidomycosis. J Clin Microbiol. 1984;20(1):103-8. https://doi.org/10.1128/jcm.20.1.103-108.1984
29. Sylvestre TF, Silva LRF, Cavalcante RS, Moris DV, Venturini J, Vicentini AP et al. Prevalence and serological diagnosis of relapse in paracoccidioidomycosis patients. PLoS Negl Trop Dis. 2014;8(5):e2834. https://doi.org/10.1371/journal.pntd.0002834
30. Beraldo KR. Comparação do perfil antigênico de Paracoccidioides brasiliensis e Paracoccidioides lutzii para o imunodiagnóstico da paracoccidioidomicose. [dissertação de mestrado]. São Paulo (SP): Coordenadoria de Controle de Doenças da Secretaria de Estado da Saúde; 2018.
31. Buccheri R, Morais VS, Kamikawa CM, Vidal MSM, Naves G, Del Negro GMB et al. Case report: misleading serological diagnosis of paracoccidioidomycosis in a young patient with the acute form disease: Paracoccidioides brasiliensis or Paracoccidioides lutzii?. Am J Trop Med Hyg. 2018;98(4):1082-85. https://doi.org/10.4269/ajtmh.17-0812
32. Salazar F, Brown GD. Antifungal innate immunity: a perspective from the last 10 years. J Innate Immun. 2018;10(5-6):373-97. https://doi.org/10.1159/000488539
33. Peron G, Fernandes FF, Landgraf TN, Martinez R, Panunto-Castelo A. Recombinant 60-kDa heat shock protein from Paracoccidioides brasiliensis: is it a good antigen for serological diagnosis of paracoccidioidomycosis? Braz J Med Biol Res. 2017;50(4):e5928. https://doi.org/10.1590/1414-431X20175928

Este trabalho está licenciado sob uma licença Creative Commons Attribution 4.0 International License.
Copyright (c) 2022 Camila Mika Kamikawa, Adriana Pardini Vicentini