Resumo
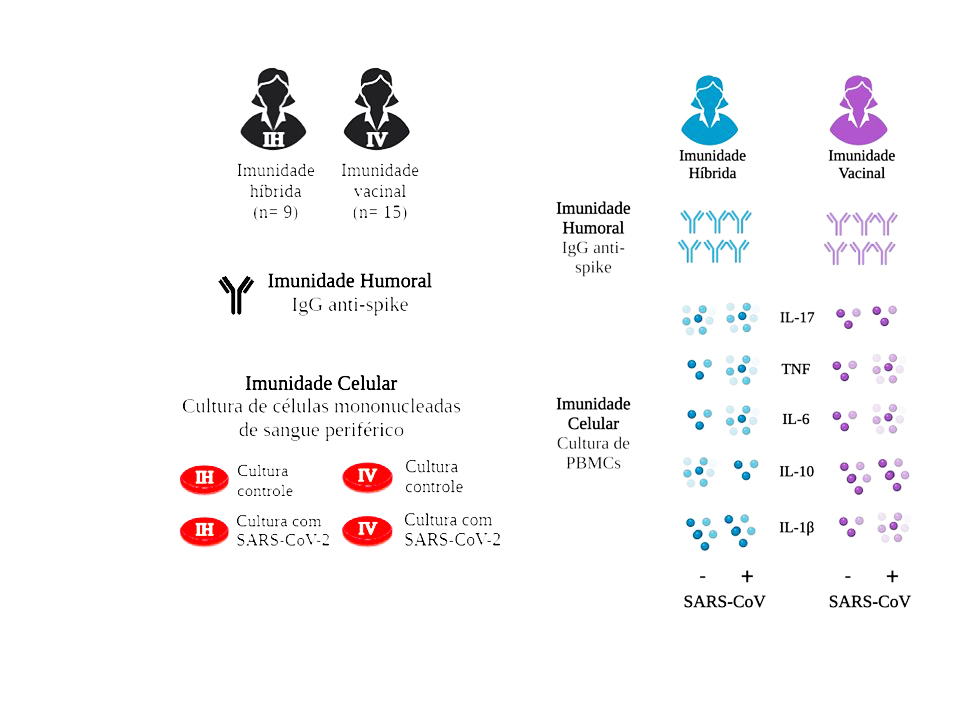
A resposta imunológica pelo SARS-CoV-2 após protocolos vacinais e infecção natural é pouco compreendida. Comparando indivíduos vacinados com esquema heterólogo que receberam um reforço vacinal (imunidade vacinal) com aqueles que apresentaram episódio leve de COVID-19 (imunidade híbrida) no mesmo período, verificamos níveis semelhantes de anticorpos contra SARS-CoV-2. Em culturas de células mononucleares, o estímulo com o antígeno viral induziu produção de citocinas pró-inflamatórias nos dois grupos, entretanto, os níveis de IL-17 foram menores em indivíduos com imunidade vacinal. Nossos resultados sugerem que o reforço vacinal teve efeitos semelhantes à infecção natural pelo SARS-CoV-2 na resposta imunológica de indivíduos previamente vacinados.
Referências
Fiolet H, Kherabi Y, MacDonald CJ, Ghosn J, Peiffer-Smadja N. Comparing COVID-19 vaccines for their characteristics, efficacy and effectiveness against SARS-CoV-2 and variants of concern: a narrative review. Clinical Microbiology and Infection. 2022;28(2):202-221. https://doi.org/10.1016/j.cmi.2021.10.005
Vespa S, Simeone P, Catitti G, Buca D, Bellis D, Pierdomenico L et al. SARS-CoV-2 and immunity: natural infection compared with vaccination. Int J Mol Sci. 2022;23:8982. https://doi.org/10.3390/ijms23168982
Hodgson SH, Mansatta K, Mallett G, Harris V, Emary KRW, Pollard AJ. What defines an efficacious COVID-19 vaccine? A review of the challenges assessing the clinical efficacy of vaccines against SARSCoV-2. Lancet Infect Dis. 2021;21(2):e26-e35. https://doi.org/10.1016/S1473-3099(20)30773-8
Rossi C, Lanuti P, Cicalini I, Bellis D, Pierdomenico L, Boccio P et al. BNT162b2 mRNA vaccination leads to long-term protection from COVID-19 disease. Vaccines. 2021;9:1164. https://doi.org/10.3390/vaccines9101164
Levin EG, Lustig Y, Cohen C, Fluss R, Indenbaum V, Amit S et al. Waning immune humoral response to BNT162b2 Covid-19 vaccine over 6 months. N Engl J Med. 2021;385(24):e84. https://doi.org/10.1056/NEJMoa2114583
Olajide OA, Iwuanyanwu VU, Adegbola OD, Al-Hindawi AA. SARS-CoV-2 spike glycoprotein S1 induces neuroinflammation in BV-2 microglia. Mol Neurobiol. 2022;59(1):445-58. https://doi.org/10.1007/s12035-021-02593-6
Wu X, Xia T, Shin WJ, Yu KM, Jung W, Herrmann A et al. Viral mimicry of Interleukin-17A by SARSCoV-2 ORF8. mBio. 2022;13(2):e00402-22. https://doi.org/10.1128/mbio.00402-22
Udomsinprasert W, Jittikoon J, Sangroongruangsri S, Chaikledkaew U. Circulating levels of Interleukin-6 and Interleukin-10, but not tumor necrosis factor-alpha, as potential biomarkers of severity and mortality for COVID-19: systematic review with meta-Analysis. J Clin Immunol. 2020;41:11-22. https://doi.org/10.1007/s10875-020-00899-z

Este trabalho está licenciado sob uma licença Creative Commons Attribution 4.0 International License.
Copyright (c) 2024 Júlia Bombini Faustini, Ana Paula Campanelli, Thais Fernanda de Campos Fraga da Silva, Vânia Nieto Brito de Souza